2023年11月30日, Nature BME在线发表美国加州理工学院汪立宏院士团队两篇背靠背论文[1,2],报道了基于光声成像的血流动力学测量新方法。12月27日,该期刊发表中国科学院深圳先进技术研究院刘成波研究员团队评述文章,对两项工作原理、价值与意义进行论述,对技术发展趋势做了展望[3]。
图 1 | News and Views 评述文章
血流动力学监测是理解人体生理与病理状态的关键,其可视化为生命功能评估和血管类疾病诊断提供了关键信息。异常血供对组织和器官造成严重损害,例如脑部血流异常会引发中风,心肌缺血会导致心脏病发作,糖尿病引起的外周血管阻塞最终导致四肢溃烂。光学成像技术包括激光多普勒、激光散斑等技术,虽然能够用于高分辨率血流成像,但它们的临床应用受到穿透深度(约1mm)的局限。光声成像,特别是光声计算层析成像技术(PACT)有效解决了这一问题。通过光能到声能的转换,PACT将成像深度拓展到厘米级,为深层血流成像提供了可能。然而,PACT在深层血流成像近年来迟迟未能突破,主要面临以下挑战。首先,PACT图像不具备散斑效应,难以对血管腔内流动信号进行测量。这一现象的根源在于血管腔内众多红细胞产生的光声信号随机抵消,因此,传统PACT只能看到血管边界。其次,在传统PACT成像中,成像速度与系统复杂度相互权衡制约,已有技术往往通过扫描单个探测器成像,牺牲了成像速度;或者使用多个探测器并行探测成像,大幅增加了系统复杂度和成本。11月30日,Nature BME在线发表的两篇背靠背论文中,报道了汪立宏院士团队的两项新技术:光声矢量断层扫描成像技术(PAVT)[1]和基于遍历继电器的光声计算断层扫描成像技术(PACTER)[2],能够有效克服PACT在深层血流成像的局限,为光声成像在血流动力学监测应用带来重大突破。
在PAVT技术中[1],研究人员利用血液内存在的空间异质性实现了深层血流成像。他们敏锐地观察到无散斑现象并非适用于全部血管,在涉及非均匀血流和血压波动的情况下,比如静脉血流中由于平滑肌收缩和单向阀门开闭产生的压力波动,就会诱发血液内产生足以被探测到的散斑信号(图2a)。利用该发现,研究人员开发出PAVT技术,成功实现了血管腔内血流信息的可视化。为了估算流速和方向,研究人员进一步分析了连续帧图像的相关性(图2b),将血液动力学信息呈现为二维血流速度矢量图(图2c)。
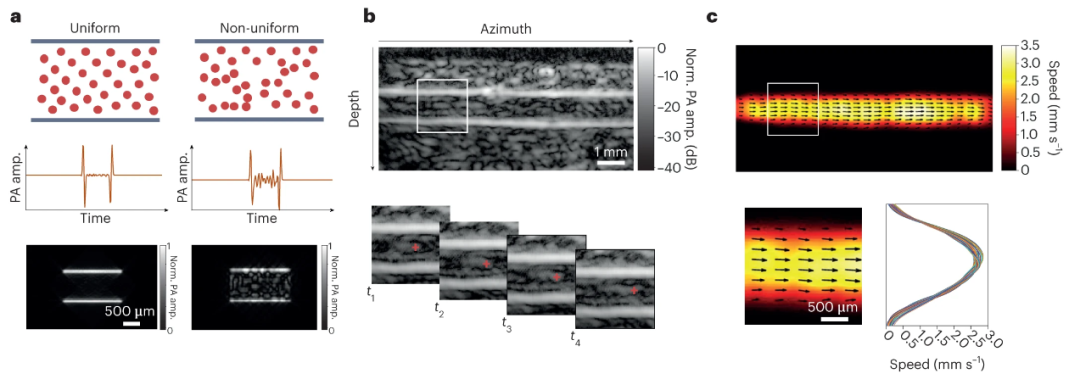
图 2 | PAVT技术。a, 腔内信号对血液异质性的依赖。均匀血液中,腔内信号振幅几乎不可见;非均匀血液中,腔内信号具有足够高的振幅可视性。b, 血管结构图实时重建。白色矩形区域的放大视图分析了连续帧图像的相关性。c, 第一行:流动矢量场叠加在二维血流速度图上。第二行:白色矩形区域放大图及其相应的速度剖面。
虽然PAVT技术首次实现了血流矢量成像,但仅限于二维图像。为了克服这一挑战,研究人员进一步开发出能够实现超快血流三维成像的单点探测技术,即PACTER[2](图3)。该技术首先采用点扫描成像对系统进行校准,该过程采用遍历继电器(ER)对光声信号波形进行时空编码(图3,a-c):每个光学焦点产生的光声信号都被其在ER腔中独特的传播路径所调制,从而具备不同特征。在这种情况下,当采用发散光束激励整个成像对象时,产生的光声信号是点扫描成像中所有焦点光声信号的线性组合,使用线性比例关系就可以提取每个聚焦点处的光声信号。在此基础上,研究人员进一步提出了虚拟探测器(VD)的概念(图3d),通过计算成像对象不同体素光声信号到达VD的传播时间延迟(图3e),反演信号三维空间位置,实现了三维血流成像。该方法不仅能够基于单次激光脉冲获得成像对象的三维图像,而且避免了传统PACT存在的系统复杂度高、成本高、尺寸大的局限。基于PACTER技术,研究人员实现了1kHz的三维成像速率,使血液动力学快速成像成为了可能。
尽管超声多普勒成像能够被用于获取深层血流信息,与之相比,PAVT在血流动力学成像方面仍具有优势。PAVT不仅可以提供光学吸收对比度,而且测量不受检测角度的限制。这使得PAVT可以应用于更加广泛的场景,例如对直径较小且流速较慢的微小血管成像。相较于PAVT,PACTER将血流动力学成像提升到了全新水平。该技术利用时空编码和VD概念实现了单点探测的快速三维成像,对于考虑探测体积限制的应用场景具有重要借鉴和推广价值,例如在便携式家庭护理监测、可穿戴医疗等领域。
综上,汪立宏院士团队报道的两项新技术为无创、无标记的人体深部血流成像提供了全新范式。该技术有助于临床血管类疾病的精准诊断,同时结合血氧代谢成像,未来还有望用于大脑功能研究。尽管如此,这些技术仍需要被优化。例如,PAVT目前仅能够对静脉血流成像,难以对空间异质性不明显的动脉血流成像。PACTER尽管在小动物和人体均实现了血流动力学三维成像,但成像质量仍有待提升。随着更多研究的开展,例如有效解决成像对象与ER之间存在的声阻抗不匹配,进一步增加ER物理覆盖尺寸,有理由相信,两种技术都将具备光明的转化应用前景。
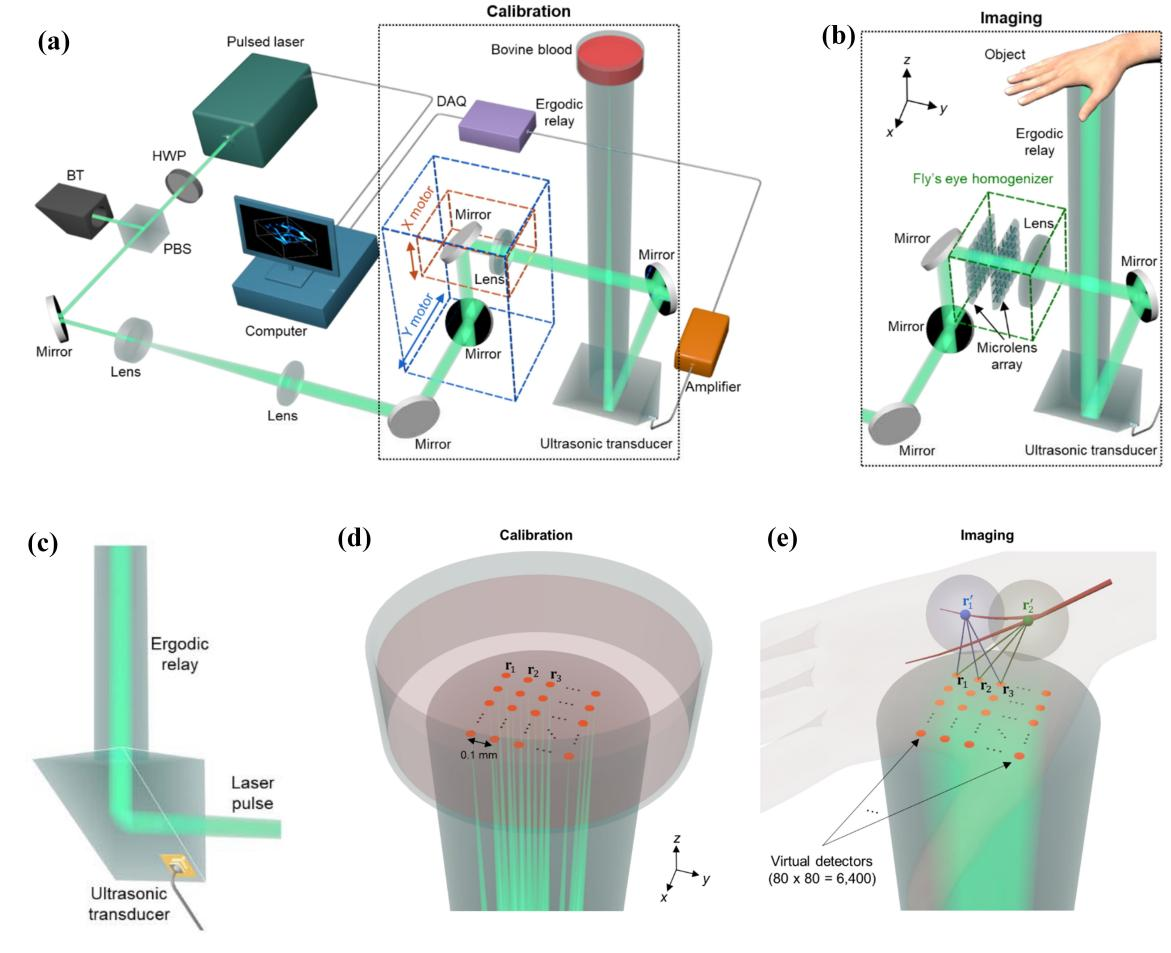
图 3 | PACTER技术。a, b, 单点扫描校准(a)和发散光束成像(b)的示意图,虚线框展示了二者区别。c, 基于ER的单阵元超声换能器探测。d, 单点扫描校准过程中的聚焦光束(绿色)与像素(橙色),后者即VD。e, PACTER在校准完成后利用发散光束(绿色)对人手血管进行成像。r1 '和r2 '代表血管内产生的光声信号源。r1, r2和r3代表VD用于捕获光声信号源(r1 '和r2 ')产生的具有不同时间延迟的信号。
参考文献
1. Yang Zhang, Joshua Olick-Gibson, Anjul Khadria, Lihong V. Wang. Nature biomedical engineering. https://doi.org/10.1038/s41551-023-01148-5.
2. Yide Zhang, Peng Hu, Lei Li, Rui Cao, Anjul Khadria, Konstantin Maslov, Xin Tong, Yushun Zeng, Laiming Jiang, Qifa Zhou, and Lihong V. Wang. Nature biomedical engineering. https://doi.org/10.1038/s41551-023-01149-4.
3. Rongkang Gao, Zhiqiang Xu, Chengbo Liu. Nature biomedical engineering. https://doi.org/10.1038/s41551-023-01162-7.